MSD ha anunciado que la Comisión Europea ha aprobado el uso de KEYTRUDA (pembrolizumab), el tratamiento anti-PD-1 de MSD, en combinación con pemetrexed (ALIMTA, de Lilly) y quimioterapia basada en platino para el tratamiento en primera línea del cáncer de pulmón no microcítico (CPNM) no escamoso metastásico en adultos cuyos tumores no tengan mutaciones positivas en EGFR o ALK. Esta aprobación, la primera en Europa de un tratamiento anti-PD-1 en combinación con quimioterapia, está basada en los datos del estudio pivotal en fase 3 KEYNOTE-189 en pacientes que presentan CPNM no escamoso metastásico, independientemente de la expresión de PD-L1. Este estudio ha mostrado beneficios del nivel de supervivencia de la combinación de pembrolizumab con quimioterapia en comparación con el tratamiento estándar de quimioterapia sola, reduciendo el riesgo de muerte en estos pacientes a la mitad (HR=0.49 [95% CI, 0.38-0.64]; p<0.00001).
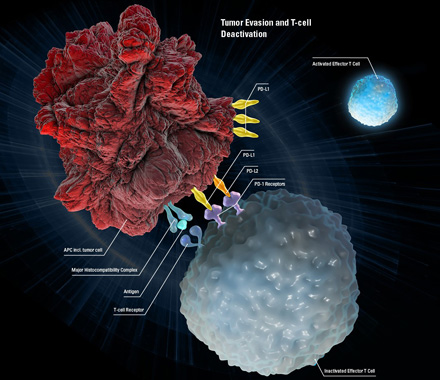
Acción del fármaco en la célula cancerígena. |
Esta aprobación permite el uso de pembrolizumab en combinación con pemetrexed y quimioterapia basada en platino en los 28 estados miembros de la UE más Islandia, Liechtenstein y Noruega, a la dosis aprobada de pembrolizumab (200 mg cada tres semanas hasta la progresión de la enfermedad o toxicidad inaceptable). En CPNM, pembrolizumab también está aprobado en Europa como monoterapia para el tratamiento de primera línea de CPNM metastásico en pacientes adultos cuyos tumores tienen alta expresión de PD-L1 –tasa de proporción del tumor (TPS) de 50% o más– sin mutaciones tumorales positivas para EGFR o ALK (KEYNOTE-024) y para pacientes adultos con CPNM localmente avanzado o metastásico previamente tratados y cuyos tumores expresan PD-L1 (TPS de 1% o más) y que han recibido al menos un régimen de quimioterapia previamente (KEYNOTE-010).
España ha jugado un papel clave en el estudio que ha motivado la nueva aprobación. Doce hospitales españoles han participado en este ensayo internacional y, además, cinco investigadores españoles figuran como firmantes de la publicación en New England Journal of Medicine (NEJM): Dr. Delvys Rodriguez (Hospital Insular de Gran Canaria); Dra. Enriqueta Felip (Hospital Vall d’Hebron de Barcelona); Dra. Belén Rubio (Hospital Quirón de Madrid); Dr. Manuel Dómine (Hospital Universitario Fundación Jiménez Díaz de Madrid; y Dr. Emilio Esteban (Hospital Universitario Central de Asturias de Oviedo).
“El resultado del estudio KEYNOTE-189 supone un avance sin precedentes en el tratamiento de los pacientes con carcinoma de pulmón no escamoso sin mutaciones de ALK o EGFR al mostrar una reducción de riesgo de muerte cuando se asocia pembrolizaumab como agente inmunomodulador al tratamiento con quimioterapia convencional con platino y pemetrexed . Consolida además el concepto de la necesidad de continuar con el tratamiento de pembrolizumab asociado a pemetrexed. Todo ello en pacientes con cualquier nivel de expresión de PD-L1”, explica el Dr. Emilio Esteban, del Hospital Universitario Central de Asturias.
En opinión del Dr. Delvys Rodriguez, máximo reclutador a nivel mundial de este estudio, la aprobación es importante, ya que, “hasta este momento estamos tratando a la mayoría de pacientes con cáncer de pulmón metastásico, no microcítico no escamoso con una combinación de platino más pemetrexed pero ya sabemos, desde que se publicaron en abril los resultados del KEYNOTE 189, que agregar pembrolizumab a esta quimioterapia ha hecho que los pacientes vivan más, de hecho en el estudio se mostró que agregar pembrolizumab reducía el riesgo de muerte en un 50% y que se beneficiaban todos los subgrupos, tantos los PD-L1 positivos como los negativos”.
En esta línea, el Dr. Manuel Dómine considera que “se cubre un hueco muy importante en los pacientes en los que la expresión de PD-L1 era negativa o inferior al 50% para los que solo disponíamos del tratamiento con quimioterapia”. “En los pacientes con expresión de PD-L1 ≥50% nos proporciona una nueva opción de tratamiento ya que actualmente disponíamos del tratamiento con pembrolizumab en monoterapia y ahora dispondremos también del uso de la combinación pembrolizumab asociado a platino-pemetrexed”, detalla el facultativo, quien incide en que esta aprobación permitirá seleccionar mejor el tratamiento para estos pacientes.